Heisann, jeg lurer på hva resultatet er ved elektrolyse av ZnSO4 i en celle og CuSO4 i en annen celle. Cellene er ikke koblet sammen.
Illustrasjon:
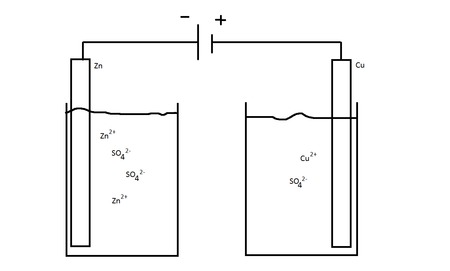
(der vi har koblet til en strømkilde på + og -)
Jeg vet at Zn2+ kommer til å feste seg til zink elektroden fordi den tar 2e- fra strømforsyningen. Og på andre siden vil det bli tatt 2e- fra kobber elektroden og vi får da Cu2+ i elektrolytten(Høyere innhold av kobber i elektrolytten).
Det jeg er litt usikker på er om H2O som er i elektrolytten blir spaltet eller om det kun gjelder hvis cellene har en kobling med hverandre?
Hvis det ikke blir spaltet, så vil vel bare S042- bli liggende igjen, men ved spalting så vil det dannes svovelsyre?
Illustrasjon:

(der vi har koblet til en strømkilde på + og -)
Jeg vet at Zn2+ kommer til å feste seg til zink elektroden fordi den tar 2e- fra strømforsyningen. Og på andre siden vil det bli tatt 2e- fra kobber elektroden og vi får da Cu2+ i elektrolytten(Høyere innhold av kobber i elektrolytten).
Det jeg er litt usikker på er om H2O som er i elektrolytten blir spaltet eller om det kun gjelder hvis cellene har en kobling med hverandre?
Hvis det ikke blir spaltet, så vil vel bare S042- bli liggende igjen, men ved spalting så vil det dannes svovelsyre?
